Проект "Роль ферментів в житті та хоз. діяльності людини "
На цій сторінці поділіться інформацією про важливі ферменти в житті живих організмів.
трипсин
Здесь мы будем собирать информацию про фермент трипсин!
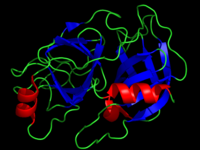
Трипсин — фермент класса гидролаз, расщепляющий пептиды и белки, обладает также эстеразной (гидролиз сложных эфиров) активностью.
Трипсины относятся к группе сериновых протеаз и содержат в активном центре остатки серина и гистидина. Трипсины легко подвергаются самоперевариванию (аутолизу), что приводит к загрязнению препаратов трипсинов неактивными продуктами (промышленный препарат содержит до 50 % неактивных примесей). Препараты трипсина высокой чистоты получают хроматографическими методами.
Физические свойства[редагувати]
Трипсин представляет собой бесцветное кристаллическое вещество с температурой плавления около 150 °C.
(Григоренко)
Биологические
свойства и функции
Основной функцией является пищеварение.
Катализирует гидролиз белков и пептидов. Может
находиться в неактивном состоянии в виде трипсиногена. Активируется, в том
числе кишечным ферментом энтеропептидазой, путём
отщепления гексапептида. Катализирует также гидролиз
восков-сложных эфиров. Оптимум каталитической активности — при pH 7,8—8.
Активный центр имеет белковую природу и состоит в основном из серина и
гистидина. Синтезируется в виде трипсиногена в
поджелудочной железе и используется в кишечнике млекопитающих и рыб.
Превращает остальные проферменты гидролаз в активные ферменты.
Применение
Трипсин используют для изготовления
лекарств. Препараты трипсина обладают противовоспалительным
и противоотёчным действием (при внутривенном и внутримышечном введении);
способны избирательно расщеплять ткани, подвергшиеся некрозу. В медицине
трипсин применяют для лечения ран, ожогов, тромбозов,
часто в сочетании с другими ферментами и с антибиотиками. Используется при
анализе первичной структуры белка, за счет того, что он селективно гидролизует
связи после остатков положительно заряженных аминокислот лизина и аргинина.
Изменение гидролитических
свойств
Активность трипсина подавляется фосфорорганическими
соединениями, некоторыми металлами, а
также рядом высокомолекулярных белковых веществ — ингибиторов
трипсина, содержащихся в тканях животных, растений и микроорганизмов.
Ионы Ca2+, Mg2+, Ba2+, Sr2+, Mn2+ повышают
гидролитическую активность трипсина.

(Вальтер)
Родственные ферменты
[редагувати]
«Ближайшие родственники» трипсина — трипсиноген, пепсин, химотрипсин. У высших животных обнаружены анионные аналоги трипсина, у многих животных и растений-нейтральные.
Медицина [редагувати]
При применении трипсина иногда могут отмечаться болезненность и гиперемия в месте введения, аллергические реакции, повышение температуры тела, тахикардия, раздражение слизистых оболочек, осиплость голоса.
Противопоказания к назначению трипсина: декомпенсация сердечной деятельности, эмфизема легких с дыхательной недостаточностью, декомпенсированные формы туберкулеза легких, дистрофия и цирроз печени, вирусный гепатит, поражения почек, панкреатит, геморрагический диатез. Трипсин нельзя вводить в очаги воспаления и кровоточащие полости, наносить на изъязвленную поверхность злокачественных опухолей.
(Клеймёнова)